Научный рук-ль: Н.И. Морозова, СУНЦ МГУ
Василиса Бобровникова (презентация)
Целью работы было синтезировать не менее двух неорганических красителей розового цвета.
В состав розовых красителей входят, в основном, органические пигменты, такие как хинакридон фуксия и нафтол красный, однако хотелось бы подобрать термически более устойчивые вещества. Неорганические пигменты в плане термостойкости проявляют себя лучше.
Для синтеза выбрали MnCl2, MnBr2 и Co(OH)2 из-за простоты их получения и доступности реактивов.
Хлорид и бромид марганца
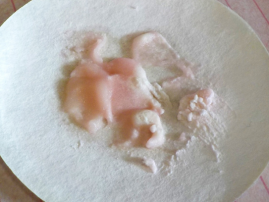
В качестве исходных веществ взяли сульфат марганца, гидрокарбонат натрия, соляную и бромоводородную кислоты. Приготовили водные растворы 6 г сульфата марганца и 2,5 г гидрокарбоната натрия в стаканах объемом 50 мл при нагревании. Слили оба раствора в стакан объемом 100 мл. Наблюдали бурное выделение газа, выпадал осадок светло-бежевого цвета. Дали осадку осесть. Отделили его декантацией. В стакане осталась взвесь с малым количеством жидкости. Разделили эту взвесь на две части, перелив половину в другой стакан. В один стакан прилили соляную кислоту, в другой – бромоводородную. Наблюдали бурное выделение газа. Получились растворы оранжево-розового цвета. Нагрели их на горелке для упаривания. После поставили остужаться. Спрятали стаканы в темное место на неделю для выпадения кристаллов. В итоге получили кристаллы дигидрата бромида марганца и застывшую пастообразную массу хлорида марганца. И то, и другое бледно-розового цвета. Уравнения протекающих реакций:
MnSO4 + 2NaHCO3 = MnCO3 + Na2SO4 + CO2 + H2O
MnCO3 + 2HCl = MnCl2 + CO2 + H2O
MnCO3 + 2HBr = MnBr2 + CO2 + H2O
Гидроксид кобальта
В качестве исходных веществ взяли гексагидрат хлорида кобальта из набора юного химика и средство для чистки труб «Крот», содержащее более 30 % гидроксида натрия. Выбор веществ был обусловлен проведением эксперимента в домашних условиях. Взвесили по 1 г каждого из исходных веществ. Растворили их в воде в двух пробирках. Получились розовый и бесцветный прозрачные растворы. Далее к раствору соли постепенно приливали «Крот». В месте контакта образовывался синий осадок, со временем розовеющий. Образующиеся наслоения выглядели, как клубы цветного дыма. Спустя некоторое время осадок и раствор стали грязно-розовыми. Осадок полностью осел. Отфильтровали его, дали высохнуть. В итоге получилось сиренево-розовое твердое вещество. Уравнение протекающей реакции:
CoCl2 ∙ 6H2O + 2NaOH = Co(OH)2 + 2NaCl + 6H2O
Итак, в ходе работы синтезировали хлорид марганца, бромид марганца, гидроксид кобальта розового цвета. Теперь их можно использовать в качестве красителей и даже делать краски на их основе.
Список литературы:
- Орлова О. В. Технология лаков и красок: Учебник для техникумов / Орлова О. В., Фомичева Т. Н. ― Москва: Химия, 1990. ― 384 с.
- Гринвуд. Химия элементов / Гринвуд Норман, Эрншо Алан. ― Москва: Издательство «БИНОМ. Лаборатория знаний», 2015 ― том 1, 607 с.
- NFPA URL: https://ru.m.wikipedia.org/wiki/NFPA_704#Реакционноспособность (Дата обращения: 11.01.2021)